


succ.: Variazioni di entropia in
..: L'entropia e il Secondo
prec.: Stati quantici
Indice
Abbiamo visto che un sistema isolato in un certo macrostato
assume l'entropia massima, cioè la configurazione con il massimo numero
di microstati (quantici) compatibili con quel macrostato. Se però
il sistema è messo in condizione di scambiare energia con l'esterno,
l'entropia cambia. Questo può avvenire in due modi:
- scambiando energia sotto forma di calore. Se trasferiamo calore
al sistema, la sua energia totale
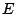 aumenta, e aumenta di conseguenza
il numero di modi in cui
aumenta, e aumenta di conseguenza
il numero di modi in cui 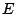 può essere distribuita tra le molecole
(il numero dei microstati); e quindi
può essere distribuita tra le molecole
(il numero dei microstati); e quindi 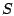 . Il contrario avviene, se
il calore passa dal sistema all'esterno:
. Il contrario avviene, se
il calore passa dal sistema all'esterno: 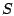 in questo caso diminuisce!
In effetti, c'è una definizione ``termodinamica'' di entropia
in base alla quale la variazione di
in questo caso diminuisce!
In effetti, c'è una definizione ``termodinamica'' di entropia
in base alla quale la variazione di 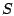 è data dal calore fornito
al sistema (in particolari condizioni, dette di reversibilità),
diviso per la temperatura:
è data dal calore fornito
al sistema (in particolari condizioni, dette di reversibilità),
diviso per la temperatura:
 |
(2) |
- scambiando energia come lavoro. È quello che avviene quando,
ad esempio, si comprime o si espande un gas in un cilindro con un
pistone. In questo modo si modifica la struttura del sistema, cioè
gli stati quantici delle molecole, ed in particolare la loro energia.
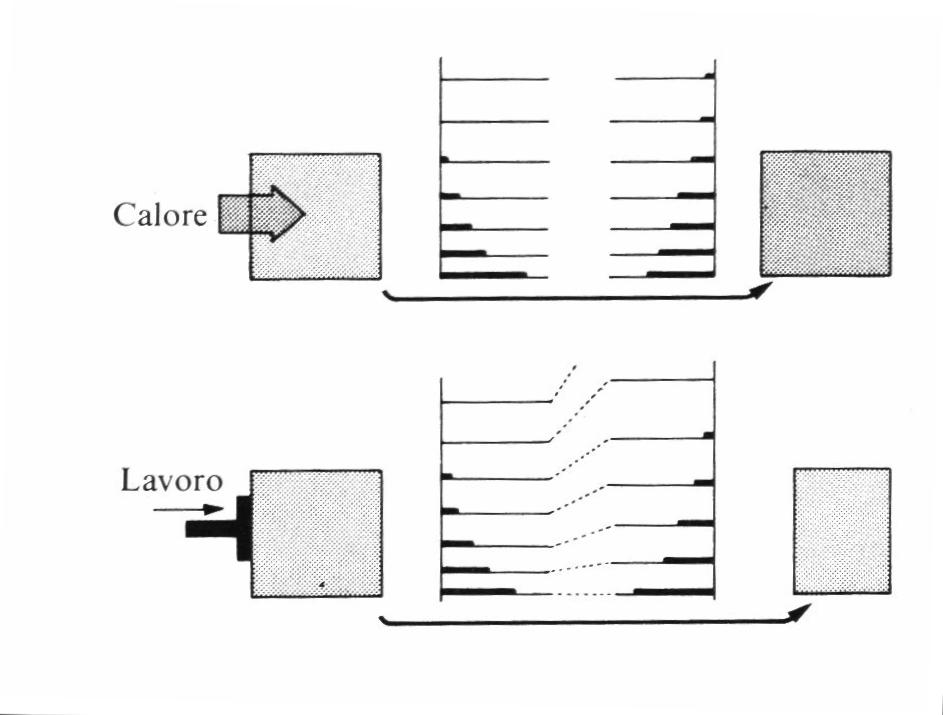
La meccanica quantistica ci dice che i livelli energetici si avvicinano
se il volume aumenta (vedi figura cap:calore-e-lavoro),
e si allontanano se il volume diminuisce. Se le popolazioni dei livelli
rimangono le stesse2, il sistema assorbe energia quando essi si allontanano (bisogna
fornire energia per comprimere un gas) e la libera quando si
avvicinano (un gas che si espande fornisce energia all'esterno). In
entrambi questi casi cambia
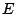 ; non cambia
; non cambia 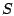 , perché il numero
di microstati rimane lo stesso. Se però permettiamo al calore di fluire
liberamente, per esempio in modo da mantenere costante la temperatura,
esso uscirà dal sistema nella compressione (l'entropia
diminuisce), e vi entrerà nell'espansione (
, perché il numero
di microstati rimane lo stesso. Se però permettiamo al calore di fluire
liberamente, per esempio in modo da mantenere costante la temperatura,
esso uscirà dal sistema nella compressione (l'entropia
diminuisce), e vi entrerà nell'espansione ( aumenta).
aumenta).
Figura:
La differenza tra calore e lavoro
 |



succ.: Variazioni di entropia in
..: L'entropia e il Secondo
prec.: Stati quantici
Indice
Giorgio F. Signorini
2006-05-24